Bạn có bao giờ tự hỏi tại sao mỗi nguyên tố lại có những đặc tính riêng biệt, không thể nhầm lẫn với bất kỳ nguyên tố nào khác? Bí mật nằm ở cấu trúc nguyên tử, mà cụ thể hơn là “dấu vân tay” của mỗi nguyên tố: số hiệu nguyên tử. Hiểu được công thức tính số hiệu nguyên tử không chỉ là kiến thức nền tảng quan trọng trong hóa học và vật lý, mà còn mở ra cánh cửa để bạn khám phá sâu hơn về thế giới vật chất quanh ta. Hãy cùng Toàn Phúc JSC đi sâu vào khái niệm này, tìm hiểu cách xác định nó và vì sao nó lại đóng vai trò then chốt trong việc phân loại và nghiên cứu các nguyên tố.
Số Hiệu Nguyên Tử Là Gì? Hiểu Rõ Khái Niệm Cốt Lõi
Số hiệu nguyên tử, thường được ký hiệu là Z, chính là số lượng proton có trong hạt nhân của một nguyên tử.
Nó không chỉ đơn thuần là một con số, mà là đặc điểm nhận dạng duy nhất của mỗi nguyên tố hóa học. Giống như mã số căn cước của bạn, không có hai nguyên tố nào có cùng số hiệu nguyên tử.
Hãy hình dung hạt nhân nguyên tử như trung tâm chỉ huy, nơi chứa các hạt proton mang điện tích dương và neutron không mang điện tích. Xung quanh hạt nhân là các electron mang điện tích âm chuyển động. Trong một nguyên tử trung hòa về điện (nghĩa là tổng điện tích dương bằng tổng điện tích âm), số electron sẽ bằng số proton. Tuy nhiên, số hiệu nguyên tử luôn luôn được xác định bởi số proton, bất kể nguyên tử đó có trung hòa điện hay không (ví dụ, khi nó trở thành ion). Số proton trong hạt nhân là bất biến đối với một nguyên tố cụ thể.
Ví dụ, Hydro (H) luôn có 1 proton trong hạt nhân, nên Z = 1. Heli (He) luôn có 2 proton, Z = 2. Oxy (O) luôn có 8 proton, Z = 8. Mỗi số hiệu nguyên tử tương ứng với một ô duy nhất trên Bảng Tuần Hoàn các Nguyên Tố Hóa Học.
Vì Sao Công Thức Tính Số Hiệu Nguyên Tử Lại Quan Trọng Đến Vậy?
Hiểu biết về cách xác định và ý nghĩa của số hiệu nguyên tử là cực kỳ quan trọng vì một số lý do cốt lõi:
- Định danh Nguyên Tố: Như đã nói, số hiệu nguyên tử là đặc trưng riêng của mỗi nguyên tố. Khi bạn biết Z, bạn sẽ biết ngay đó là nguyên tố nào. Điều này là nền tảng cho mọi nghiên cứu và ứng dụng hóa học, từ phân tích thành phần vật liệu đến tổng hợp chất mới.
- Cơ Sở Của Bảng Tuần Hoàn: Bảng Tuần Hoàn được sắp xếp dựa trên số hiệu nguyên tử tăng dần. Việc sắp xếp này không chỉ là thứ tự các nguyên tố mà còn phản ánh sự thay đổi tuần hoàn về cấu hình electron và tính chất hóa học của chúng. Z chính là chìa khóa để hiểu cấu trúc và cách sử dụng Bảng Tuần Hoàn.
- Xác Định Cấu Trúc Nguyên Tử: Từ số hiệu nguyên tử, bạn có thể suy ra số electron trong nguyên tử trung hòa (bằng Z). Cấu hình electron của một nguyên tử quyết định tính chất hóa học, khả năng hình thành liên kết, và nhiều đặc điểm khác của nguyên tố đó.
- Hiểu Về Hạt Nhân: Z cho biết số lượng hạt cơ bản quan trọng nhất trong hạt nhân – proton. Cùng với số neutron, nó quyết định số khối và ảnh hưởng đến tính bền vững của hạt nhân, cũng như các tính chất hạt nhân (như tính phóng xạ).
Việc nắm vững công thức tính số hiệu nguyên tử và ý nghĩa của nó giống như việc bạn học bảng chữ cái trước khi đọc sách vậy. Nó là bước đi đầu tiên và quan trọng nhất trên con đường khám phá thế giới hóa học đầy fascinating.
Công Thức Tính Số Hiệu Nguyên Tử: Nền Tảng Cần Nắm Vững
Thực tế, nói về “công thức” để tính số hiệu nguyên tử có thể hơi quá lời, bởi nó không phải là một phép tính phức tạp với nhiều biến số. Số hiệu nguyên tử (Z) về bản chất đã được định nghĩa là số proton (p) trong hạt nhân.
Công thức đơn giản nhất và cốt lõi nhất là:
Z = p
Trong đó:
- Z là Số hiệu nguyên tử
- p là Số proton trong hạt nhân
Tuy nhiên, trong thực tế, chúng ta không phải lúc nào cũng được cho trực tiếp số proton. Chúng ta có thể được cung cấp các thông tin khác về nguyên tử và cần suy luận ra số proton, từ đó xác định Z. Dưới đây là các “công thức” hay đúng hơn là các phương pháp xác định số hiệu nguyên tử dựa trên các thông tin khác nhau:
-
Dựa vào số electron (đối với nguyên tử trung hòa):
Trong một nguyên tử trung hòa về điện, số electron (e) bằng số proton (p).
Vì vậy, đối với nguyên tử trung hòa:
Z = p = e
Nếu đề bài cho biết một nguyên tử X trung hòa có 10 electron, thì số proton của nó là 10. Suy ra, số hiệu nguyên tử Z = 10. Tra bảng tuần hoàn, Z=10 là nguyên tố Neon (Ne). Lưu ý quan trọng: Công thức này chỉ áp dụng cho nguyên tử trung hòa. Đối với ion (nguyên tử đã nhường hoặc nhận electron và mang điện tích), số electron sẽ khác số proton. -
Dựa vào số khối và số neutron:
Số khối (A), còn gọi là số khối nguyên tử, là tổng số proton (p) và số neutron (n) trong hạt nhân của một nguyên tử.
A = p + n
Từ công thức này, chúng ta có thể suy ra số proton:
p = A – n
Vì Z = p, nên:
Z = A – n
Ví dụ: Một đồng vị của nguyên tố X có số khối A = 35 và số neutron n = 18. Số proton p = A – n = 35 – 18 = 17. Số hiệu nguyên tử Z = 17. Đây là nguyên tố Clo (Cl). Việc hiểu mối quan hệ giữa số khối, số proton và số neutron giúp chúng ta xác định nguyên tố ngay cả khi không biết trực tiếp số proton. -
Dựa vào vị trí trên Bảng Tuần Hoàn:
Đây là cách phổ biến và đơn giản nhất trong thực tế. Bảng Tuần Hoàn các Nguyên Tố Hóa Học được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử. Số thứ tự của nguyên tố trong Bảng Tuần Hoàn chính là số hiệu nguyên tử của nó.
Ví dụ: Nguyên tố ở ô số 6 trên Bảng Tuần Hoàn là Carbon (C), có số hiệu nguyên tử Z = 6. Nguyên tố ở ô số 26 là Sắt (Fe), có Z = 26. Cách này cực kỳ hữu ích khi bạn có Bảng Tuần Hoàn trong tay.
Việc nắm vững các phương pháp này giúp bạn linh hoạt xác định số hiệu nguyên tử dù thông tin ban đầu được cho dưới dạng nào. Quan trọng nhất vẫn là hiểu rằng Z luôn luôn bằng số proton. Các phương pháp khác chỉ là cách suy luận ra số proton từ thông tin gián tiếp.
 Hình ảnh mô phỏng cấu tạo nguyên tử với hạt nhân chứa proton và neutron, và electron quay quanh, minh họa số proton là số hiệu nguyên tử
Hình ảnh mô phỏng cấu tạo nguyên tử với hạt nhân chứa proton và neutron, và electron quay quanh, minh họa số proton là số hiệu nguyên tử
Làm Thế Nào Để Xác Định Số Hiệu Nguyên Tử Trong Các Trường Hợp Khác Nhau?
Như đã đề cập ở trên, tùy thuộc vào thông tin bạn có, sẽ có những cách tiếp cận khác nhau để tìm ra số hiệu nguyên tử (Z).
Câu hỏi thường gặp: Làm sao để biết số hiệu nguyên tử khi chỉ có một vài thông tin về nguyên tử?
Trả lời ngắn gọn: Dựa vào số proton (luôn luôn), hoặc suy luận số proton từ số electron (nếu trung hòa), số khối và số neutron, hoặc đơn giản nhất là tra vị trí trên Bảng Tuần Hoàn.
Chúng ta hãy đi sâu hơn vào từng trường hợp với các ví dụ cụ thể:
Trường Hợp 1: Biết Số Proton
Đây là trường hợp trực tiếp nhất. Vì số hiệu nguyên tử được định nghĩa là số proton, nên nếu bạn biết số proton, bạn đã biết ngay số hiệu nguyên tử.
- Ví dụ: Nguyên tử Natri (Na) có hạt nhân chứa 11 proton.
- Số proton (p) = 11
- Theo định nghĩa, Số hiệu nguyên tử (Z) = p = 11.
- Kết luận: Số hiệu nguyên tử của Natri là 11.
Trường hợp này thường xuất hiện trong các bài toán lý thuyết hoặc khi giới thiệu khái niệm cơ bản.
Trường Hợp 2: Biết Số Electron (và là Nguyên Tử Trung Hòa)
Nếu bạn được cho biết số electron của một nguyên tử và biết chắc chắn rằng nguyên tử đó trung hòa về điện (không phải là ion), thì bạn có thể suy ra số proton.
-
Ví dụ: Một nguyên tử X trung hòa có 17 electron.
- Vì nguyên tử X trung hòa, số electron (e) = số proton (p).
- e = 17 => p = 17.
- Số hiệu nguyên tử (Z) = p = 17.
- Kết luận: Số hiệu nguyên tử của nguyên tử X là 17. Tra Bảng Tuần Hoàn, Z=17 là nguyên tố Clo (Cl).
-
Lưu ý: Nếu đề bài chỉ nói “ion X có 18 electron” mà không cho biết nó là ion dương hay âm, mang bao nhiêu điện tích, thì bạn không thể dùng số electron để xác định số proton. Ví dụ, ion Cl⁻ có 18 electron, nhưng số proton của Clo vẫn là 17. Ion Na⁺ có 10 electron, nhưng số proton của Natri vẫn là 11.
Trường Hợp 3: Biết Số Khối và Số Neutron
Đây là trường hợp phổ biến khi làm việc với các đồng vị hoặc các bài toán về hạt nhân nguyên tử.
-
Ví dụ: Một đồng vị của nguyên tố Y có số khối A = 40 và số neutron n = 20.
- Ta có công thức: Số khối (A) = Số proton (p) + Số neutron (n).
- Suy ra: Số proton (p) = A – n.
- p = 40 – 20 = 20.
- Số hiệu nguyên tử (Z) = p = 20.
- Kết luận: Số hiệu nguyên tử của nguyên tố Y là 20. Tra Bảng Tuần Hoàn, Z=20 là nguyên tố Canxi (Ca).
-
Ví dụ khác: Đồng vị Carbon-14 (¹⁴C) có số khối A = 14 và Carbon có số proton Z=6. Số neutron trong ¹⁴C là bao nhiêu?
- Ở đây đề bài cho Z và A, yêu cầu tìm n.
- Ta có Z = p = 6.
- A = p + n => n = A – p = A – Z.
- n = 14 – 6 = 8.
- Kết luận: Đồng vị Carbon-14 có 8 neutron (trong khi đồng vị Carbon-12 phổ biến hơn có 12-6=6 neutron). Số proton (và Z) của cả hai đồng vị này đều là 6, đúng là cùng một nguyên tố Carbon.
Trường Hợp 4: Dựa vào Vị Trí trên Bảng Tuần Hoàn
Đây là cách thường dùng nhất trong phòng thí nghiệm hoặc khi học tập. Bảng Tuần Hoàn là công cụ không thể thiếu.
- Ví dụ: Bạn tìm thấy nguyên tố Kẽm (Zn) trên Bảng Tuần Hoàn.
- Quan sát vị trí của Kẽm trên Bảng Tuần Hoàn. Nó nằm ở ô số 30.
- Số thứ tự của nguyên tố trong Bảng Tuần Hoàn chính là số hiệu nguyên tử của nó.
- Kết luận: Số hiệu nguyên tử của Kẽm (Zn) là Z = 30. Điều này có nghĩa là mỗi nguyên tử Kẽm có 30 proton trong hạt nhân.
Khi bạn đã quen thuộc với Bảng Tuần Hoàn, việc xác định số hiệu nguyên tử trở nên cực kỳ nhanh chóng và dễ dàng. Bảng Tuần Hoàn cũng cung cấp nhiều thông tin hữu ích khác như tên nguyên tố, ký hiệu, số khối trung bình, và đôi khi cả cấu hình electron sơ bộ. Việc liên hệ số hiệu nguyên tử với vị trí trong bảng giúp củng cố sự hiểu biết của bạn về mối quan hệ giữa cấu trúc nguyên tử và tính chất của nguyên tố.
Có thể bạn quan tâm: để chuyển đổi giữa các đơn vị đo lường khác nhau trong vật lý và hóa học, bạn có thể cần biết 1" bằng bao nhiêu cm. Hiểu rõ các đơn vị đo lường cơ bản là rất quan trọng khi làm việc với các khái niệm vật lý liên quan đến kích thước nguyên tử hay khoảng cách giữa các hạt.
Các Lầm Tưởng Thường Gặp Khi Áp Dụng Công Thức Tính Số Hiệu Nguyên Tử
Khi mới bắt đầu học về cấu tạo nguyên tử, không ít người dễ mắc phải một vài nhầm lẫn cơ bản. Việc nhận diện và tránh những sai lầm này sẽ giúp bạn nắm vững kiến thức hơn về công thức tính số hiệu nguyên tử.
Câu hỏi thường gặp: Những sai lầm phổ biến nào cần tránh khi xác định số hiệu nguyên tử?
Trả lời ngắn gọn: Nhầm lẫn số hiệu nguyên tử với số khối, áp dụng quy tắc Z=e cho ion, hoặc không phân biệt rõ giữa proton và neutron.
Dưới đây là những lầm tưởng phổ biến nhất:
-
Nhầm lẫn Số Hiệu Nguyên Tử (Z) và Số Khối (A):
- Lầm tưởng: Số hiệu nguyên tử là tổng số hạt trong hạt nhân.
- Sự thật: Số hiệu nguyên tử (Z) chỉ là số proton. Số khối (A) mới là tổng số proton và neutron (A = p + n). Đây là sự nhầm lẫn phổ biến nhất. Hãy nhớ: Z định danh nguyên tố, A định danh đồng vị cụ thể của nguyên tố đó. Carbon luôn có Z=6, nhưng có thể là đồng vị Carbon-12 (A=12), Carbon-13 (A=13), Carbon-14 (A=14), v.v.
-
Áp dụng quy tắc Z = e cho Ion:
- Lầm tưởng: Số electron luôn bằng số hiệu nguyên tử.
- Sự thật: Chỉ đúng cho nguyên tử trung hòa. Ion là nguyên tử đã nhường (tạo ion dương) hoặc nhận (tạo ion âm) electron, nên số electron của ion khác số proton. Số hiệu nguyên tử (Z) luôn luôn bằng số proton, không thay đổi khi nguyên tử trở thành ion.
- Ví dụ: Nguyên tử Oxy (O) có Z=8 (8 proton, 8 electron khi trung hòa). Khi nhận 2 electron để tạo thành ion O²⁻, nó có 8 proton nhưng 10 electron. Số hiệu nguyên tử của Oxy vẫn là 8.
-
Không phân biệt rõ Proton và Neutron:
- Lầm tưởng: Proton và neutron là giống nhau.
- Sự thật: Cả hai đều là hạt nhân, nhưng proton mang điện tích dương và xác định nguyên tố (qua Z), trong khi neutron không mang điện tích và ảnh hưởng đến số khối (A) và tính bền vững của hạt nhân (tạo ra các đồng vị).
-
Đọc sai thông tin trên Bảng Tuần Hoàn:
- Lầm tưởng: Con số lớn nhất ghi dưới ký hiệu nguyên tố trên Bảng Tuần Hoàn là số hiệu nguyên tử.
- Sự thật: Tùy cách trình bày của Bảng Tuần Hoàn, nhưng số ghi phía trên ký hiệu nguyên tố (thường là số nguyên nhỏ) mới là số hiệu nguyên tử (số thứ tự). Con số thập phân lớn hơn thường là số khối trung bình (khối lượng nguyên tử) của nguyên tố đó, tính trung bình các đồng vị tự nhiên.
Việc cẩn thận với định nghĩa và biết rõ khi nào áp dụng công thức Z=e là rất quan trọng để tránh sai sót khi làm bài tập hay nghiên cứu.
Trong các lĩnh vực kỹ thuật, đặc biệt là điện, việc tính toán các đại lượng như điện trở, dòng điện, hiệu điện thế là nền tảng. Bạn có thể tham khảo về công thức định luật ôm để hiểu rõ hơn về mối quan hệ giữa các đại lượng này, tương tự như cách chúng ta tìm hiểu mối quan hệ giữa các hạt cơ bản trong nguyên tử để xác định số hiệu nguyên tử.
Áp Dụng Thực Tế: Số Hiệu Nguyên Tử Giúp Ích Gì Cho Chúng Ta?
Kiến thức về số hiệu nguyên tử không chỉ nằm trên sách vở hay trong các bài kiểm tra. Nó có vô số ứng dụng thực tế trong nhiều lĩnh vực khoa học và công nghệ khác nhau.
Câu hỏi thường gặp: Số hiệu nguyên tử được ứng dụng trong đời sống và khoa học như thế nào?
Trả lời ngắn gọn: Từ y học, công nghiệp, nghiên cứu vật liệu đến năng lượng hạt nhân, số hiệu nguyên tử đóng vai trò quan trọng trong việc hiểu và sử dụng các nguyên tố.
Dưới đây là một vài ví dụ điển hình:
-
Trong Hóa Học và Khoa Học Vật Liệu:
- Xác định và tổng hợp vật liệu mới: Dựa vào số hiệu nguyên tử, các nhà khoa học có thể dự đoán tính chất hóa học của các nguyên tố và cách chúng sẽ tương tác với nhau để tạo ra các hợp chất có tính chất mong muốn (ví dụ: vật liệu bán dẫn, polyme, vật liệu siêu dẫn).
- Kiểm soát chất lượng: Phân tích thành phần hóa học của mẫu vật thường bắt đầu bằng việc xác định các nguyên tố có mặt, điều này dựa vào số hiệu nguyên tử của chúng. Các kỹ thuật như phổ khối (mass spectrometry) hay phổ phát xạ nguyên tử (atomic emission spectroscopy) đều liên quan đến việc xác định nguyên tố dựa trên các đặc trưng liên quan đến Z.
-
Trong Y Học:
- Y học hạt nhân và chẩn đoán hình ảnh: Các đồng vị phóng xạ của các nguyên tố (có cùng Z nhưng khác A) được sử dụng rộng rãi trong chẩn đoán và điều trị. Ví dụ, I-131 (đồng vị của Iốt, Z=53) dùng để chẩn đoán và điều trị bệnh tuyến giáp; Technetium-99m (đồng vị của Technetium, Z=43) dùng trong nhiều kỹ thuật quét y học. Việc hiểu số hiệu nguyên tử giúp xác định nguyên tố phù hợp cho từng ứng dụng.
- Xạ trị: Việc sử dụng các tia X hoặc tia gamma để điều trị ung thư cũng liên quan đến tương tác của bức xạ với nguyên tử trong tế bào. Tương tác này phụ thuộc vào số hiệu nguyên tử của các nguyên tố cấu thành mô.
-
Trong Vật Lý Hạt Nhân và Năng Lượng:
- Thiết kế lò phản ứng hạt nhân: Nhiên liệu hạt nhân phổ biến là Uranium (Z=92). Việc hiểu số proton (Z) và số neutron (n) trong các đồng vị Uranium (như U-235, U-238) là cốt lõi để kiểm soát phản ứng phân hạch dây chuyền và sản xuất năng lượng.
- Nghiên cứu các nguyên tố siêu nặng: Các nguyên tố mới được tạo ra trong phòng thí nghiệm được định danh bằng số hiệu nguyên tử của chúng, dựa trên số proton trong hạt nhân được tổng hợp. Đây là lĩnh vực nghiên cứu đỉnh cao về cấu trúc hạt nhân.
-
Trong Pháp Y và Phân Tích:
- Phân tích mẫu vật tại hiện trường: Các kỹ thuật phân tích nguyên tố dựa trên số hiệu nguyên tử giúp xác định thành phần của thuốc nổ, ma túy, hoặc các vật liệu liên quan đến vụ án.
- Xác định nguồn gốc vật liệu: Phân tích thành phần nguyên tố có thể giúp truy nguyên nguồn gốc của các vật liệu như quặng, đất, hoặc thậm chí là các sản phẩm giả mạo.
Những ứng dụng này cho thấy số hiệu nguyên tử không chỉ là một khái niệm trừu tượng mà là một công cụ mạnh mẽ giúp chúng ta hiểu, kiểm soát và tận dụng thế giới nguyên tử vì lợi ích của con người.
Khi nói về các đơn vị đo lường trong vật lý, chúng ta biết rằng chúng rất đa dạng. Việc hiểu rõ các chuyển đổi đơn vị là cần thiết cho tính toán chính xác. Tương tự, trong lĩnh vực năng lượng, có những khái niệm và công thức cơ bản mà bất cứ ai làm việc trong ngành cũng cần nắm vững, chẳng hạn như mối liên hệ giữa khối lượng và năng lượng, biểu thị qua mc bằng bao nhiêu c.
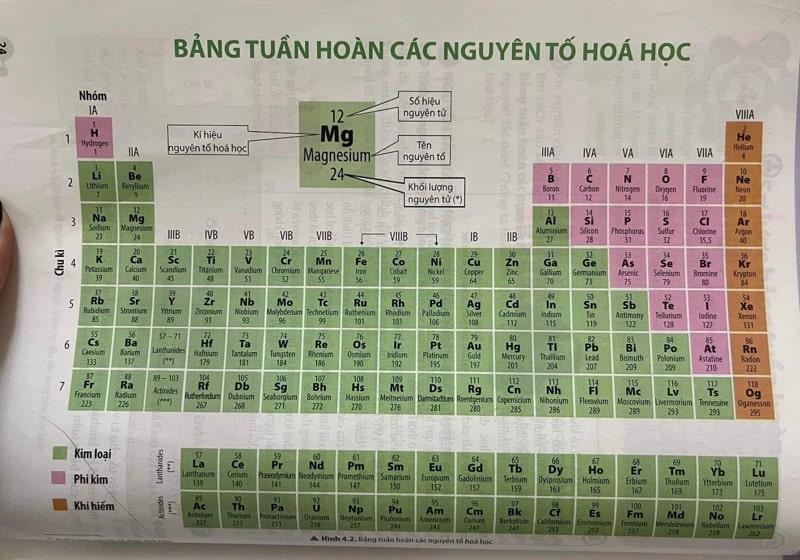 Bảng tuần hoàn các nguyên tố hóa học, làm nổi bật số hiệu nguyên tử của mỗi nguyên tố
Bảng tuần hoàn các nguyên tố hóa học, làm nổi bật số hiệu nguyên tử của mỗi nguyên tố
Lời Khuyên Từ Chuyên Gia Khi Làm Việc Với Các Khái Niệm Nguyên Tử
Để giúp bạn học tập và làm việc hiệu quả hơn với khái niệm số hiệu nguyên tử và các khái niệm liên quan, chúng tôi đã tham khảo ý kiến của Tiến sĩ Phan Thu Hà, một chuyên gia Hóa học Vật liệu có nhiều năm kinh nghiệm giảng dạy và nghiên cứu.
Tiến sĩ Phan Thu Hà chia sẻ:
“Khi tiếp cận cấu tạo nguyên tử, điều cốt lõi là phải hiểu rõ định nghĩa của từng loại hạt: proton, neutron, electron. Số hiệu nguyên tử Z chính là ‘linh hồn’ của nguyên tố, chỉ phụ thuộc vào số proton. Đừng để bị phân tâm bởi số electron trong ion hay số neutron trong đồng vị khi xác định nguyên tố. Bảng Tuần Hoàn là người bạn đồng hành tốt nhất của bạn, hãy sử dụng nó thật hiệu quả.”
Tiến sĩ Hà nhấn mạnh tầm quan trọng của việc thực hành và làm bài tập:
“Lý thuyết là nền tảng, nhưng chỉ khi áp dụng vào giải quyết các bài toán cụ thể, bạn mới thực sự nắm vững được công thức tính số hiệu nguyên tử trong các tình huống khác nhau. Hãy thử sức với các bài tập xác định Z từ số khối và neutron, hoặc từ số electron của nguyên tử trung hòa. Dần dần, bạn sẽ thấy việc này trở nên đơn giản như hơi thở vậy.”
Những lời khuyên từ chuyên gia giúp chúng ta thấy rằng việc học hóa học, vật lý không chỉ là ghi nhớ công thức mà còn là hiểu sâu sắc ý nghĩa của chúng và cách áp dụng linh hoạt. Sự cẩn thận, thực hành thường xuyên và sử dụng các công cụ hỗ trợ như Bảng Tuần Hoàn là chìa khóa để thành công.
Trong hóa học và vật lý, chúng ta thường xuyên làm việc với các đại lượng mang điện. Khái niệm điện tích đơn vị là gì là một trong những khái niệm cơ bản nhất liên quan đến điện tích của các hạt như proton và electron, những hạt cấu thành nên nguyên tử mà chúng ta đang nói tới. Hiểu về điện tích đơn vị giúp ta lý giải tại sao nguyên tử trung hòa khi số proton bằng số electron, và tại sao ion lại mang điện.
Các Câu Hỏi Thường Gặp Về Số Hiệu Nguyên Tử
Để củng cố thêm kiến thức và giải đáp những thắc mắc phổ biến, chúng ta hãy cùng trả lời một số câu hỏi thường gặp về số hiệu nguyên tử.
Số hiệu nguyên tử có bao giờ thay đổi không?
Trả lời ngắn gọn: Số hiệu nguyên tử của một nguyên tử chỉ thay đổi khi số proton trong hạt nhân thay đổi, điều này chỉ xảy ra trong các phản ứng hạt nhân hoặc phân rã phóng xạ, biến nguyên tử này thành nguyên tử của nguyên tố khác.
Giải thích chi tiết hơn: Trong các phản ứng hóa học thông thường, chỉ có sự trao đổi hoặc dùng chung electron ở lớp vỏ nguyên tử. Hạt nhân nguyên tử (và do đó số proton) không thay đổi. Vì vậy, số hiệu nguyên tử của nguyên tố tham gia phản ứng hóa học vẫn giữ nguyên. Chỉ trong các phản ứng hạt nhân (như phân hạch, nhiệt hạch, hoặc phân rã phóng xạ alpha, beta), số proton trong hạt nhân mới có thể thay đổi, dẫn đến sự biến đổi từ nguyên tố này sang nguyên tố khác. Ví dụ, khi Uranium-238 (Z=92) phân rã alpha, nó mất đi 2 proton, trở thành Thorium-234 (Z=90).
Nguyên tử trung hòa là gì?
Trả lời ngắn gọn: Nguyên tử trung hòa là nguyên tử mà tổng điện tích dương của các proton trong hạt nhân bằng tổng điện tích âm của các electron ở lớp vỏ, tức là số proton bằng số electron.
Giải thích chi tiết hơn: Proton mang điện tích dương (+1e, với e là điện tích đơn vị cơ bản), electron mang điện tích âm (-1e), còn neutron không mang điện tích. Một nguyên tử được gọi là trung hòa về điện khi số lượng proton (p) bằng số lượng electron (e). Khi đó, tổng điện tích dương (+pe) cân bằng với tổng điện tích âm (-ee), khiến nguyên tử không mang điện tích ròng.
Làm sao phân biệt số hiệu nguyên tử và số khối?
Trả lời ngắn gọn: Số hiệu nguyên tử (Z) là số proton, xác định nguyên tố. Số khối (A) là tổng số proton và neutron, xác định đồng vị cụ thể.
Giải thích chi tiết hơn: Điểm khác biệt cốt lõi là số hạt được tính. Z chỉ đếm proton. A đếm cả proton và neutron. Hai nguyên tử có cùng Z chắc chắn là cùng một nguyên tố, nhưng có thể khác A nếu số neutron khác nhau (gọi là đồng vị). Hai nguyên tử có cùng A nhưng khác Z chắc chắn là hai nguyên tố khác nhau (và cũng sẽ có số neutron khác nhau). Ví dụ, Carbon-12 (Z=6, A=12, n=6) và Carbon-14 (Z=6, A=14, n=8) là đồng vị của Carbon. Còn Carbon-12 và Nitơ-14 (Z=7, A=14, n=7) là hai nguyên tố khác nhau dù có cùng số khối A=14.
Bảng tuần hoàn có liên quan gì đến số hiệu nguyên tử?
Trả lời ngắn gọn: Bảng Tuần Hoàn được sắp xếp chủ yếu theo thứ tự tăng dần của số hiệu nguyên tử và là công cụ chính để tìm số hiệu nguyên tử của một nguyên tố.
Giải thích chi tiết hơn: Mỗi nguyên tố trên Bảng Tuần Hoàn chiếm một ô duy nhất, và số thứ tự của ô đó (thường được ghi rõ) chính là số hiệu nguyên tử của nguyên tố đó. Sự sắp xếp này phản ánh quy luật tuần hoàn về cấu hình electron và tính chất hóa học khi số proton tăng lên. Bảng Tuần Hoàn là một hệ thống khoa học tuyệt vời, tổng hợp thông tin quan trọng về mọi nguyên tố dựa trên số hiệu nguyên tử của chúng.
Việc làm rõ những câu hỏi này giúp củng cố sự hiểu biết về các khái niệm cơ bản liên quan đến cấu tạo nguyên tử và công thức tính số hiệu nguyên tử, giúp bạn tự tin hơn khi học sâu hơn về hóa học và vật lý.
Trong lĩnh vực vật lý, đặc biệt là nhiệt học, khái niệm nhiệt dung riêng của một chất là gì giúp chúng ta hiểu về khả năng hấp thụ và giữ nhiệt của các vật liệu khác nhau. Khả năng này cũng phụ thuộc vào bản chất nguyên tố cấu thành vật liệu, mà bản chất nguyên tố lại được xác định bởi số hiệu nguyên tử của chúng.
Kết Luận
Qua hành trình khám phá này, chúng ta đã cùng nhau tìm hiểu công thức tính số hiệu nguyên tử – một khái niệm tưởng chừng đơn giản nhưng lại là nền tảng cho toàn bộ ngành hóa học và nhiều lĩnh vực khoa học khác. Chúng ta đã thấy rằng số hiệu nguyên tử (Z) không chỉ đơn thuần là số thứ tự trên Bảng Tuần Hoàn, mà chính là số proton trong hạt nhân, “dấu vân tay” độc nhất vô nhị để định danh từng nguyên tố.
Bạn đã biết cách xác định số hiệu nguyên tử dựa trên số proton, số electron (đối với nguyên tử trung hòa), số khối và số neutron, hay đơn giản nhất là tra cứu trên Bảng Tuần Hoàn. Chúng ta cũng đã chỉ ra những lầm tưởng phổ biến cần tránh và cùng nhau xem xét vô vàn ứng dụng thực tế của kiến thức này, từ y học, công nghiệp đến nghiên cứu khoa học đỉnh cao.
Việc nắm vững công thức tính số hiệu nguyên tử và ý nghĩa sâu sắc của nó không chỉ giúp bạn giải quyết các bài tập hóa học dễ dàng hơn mà còn mở ra một góc nhìn mới về cách thế giới vật chất được cấu tạo. Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích, giúp bạn tự tin hơn trên con đường chinh phục tri thức khoa học.
Đừng ngần ngại áp dụng những kiến thức này vào thực tế, đặt câu hỏi khi chưa rõ và tìm hiểu sâu hơn về những nguyên tố mà bạn cảm thấy hứng thú. Thế giới nguyên tử luôn chứa đựng những điều bất ngờ đang chờ bạn khám phá! Kiến thức về công thức tính số hiệu nguyên tử chính là viên gạch đầu tiên cho những khám phá tuyệt vời đó.

